H2O2工作液的工作原理(一)
仔细分析工作液的整个反应,我们发现加氢环节才是过氧化氢制备过程中的核心环节。理想的AO反应中氢的转移过程是一个奇特的反应,每完成一次还原/氧化的循环,只能在蒽醌分子中引入一个分子的氢,而且这两个氢原子将分别结合于蒽醌结构
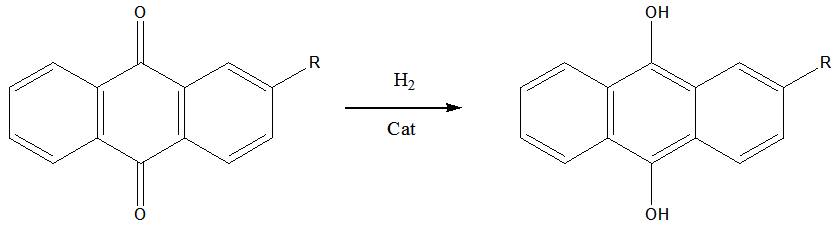
中的两个羰基氧上,如果加氢反应偏离了这个反应方向,所得产物就将完全或者部分失去其氧化活性,工作液的有效成分就会发生变化,从而影响到整个反应中氢效的计算。因此,加氢反应必须保证不破坏蒽醌的醌式结构才能保证氢转移、氢醌氧化反应的正常进行。其反应机理可能为:氢自由基进攻蒽醌的一个羰基,该羰基双键打开后电子重新排布得到一个新的自由基,与另一个氢自由基结合后获得氢化蒽醌。氧化过程中氢化蒽醌受分子氧进攻,酚羟基上的氢自由基被氧分子夺取,生成
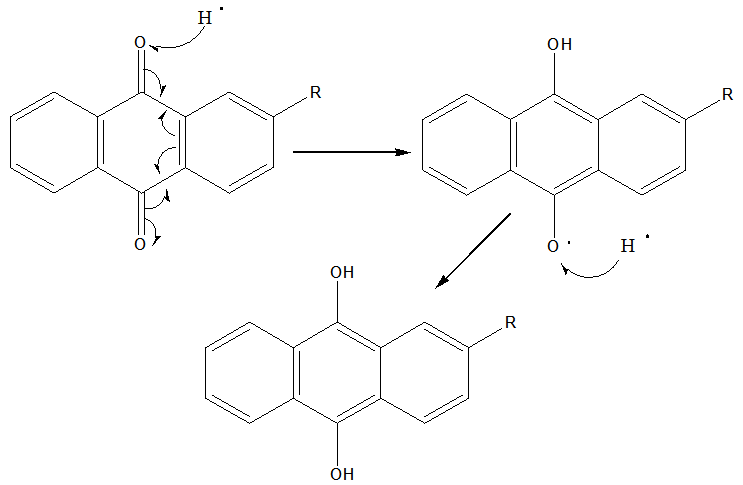
一个半醌式自由基;氧分子获得氢自由基后转变成过氧氢自由基,过氧氢自由基进攻半醌式自由基结构中的另一个酚羟基,从中获取氢自由基后生成过氧化氢,半醌式自由基则转变为全醌式双自由基,该中间体不稳定,经电子重排后转变为蒽醌,工作液中的主成分蒽醌经一次还原、一次氧化后完成一个完整循环,生成一分子过氧化氢。所以工作液保持活性的前提就是
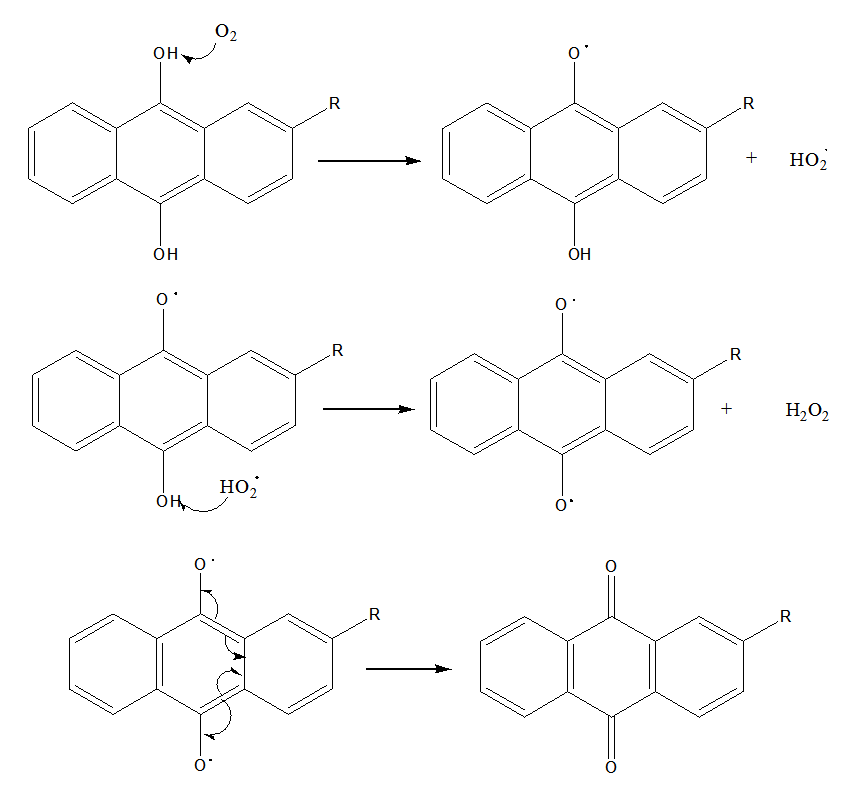
能够一直将这个循环过程重复下去,这对蒽醌加氢过程中使用催化剂的选择性要求很高,每完成一次循环只能消耗一分子氢,这两个氢原子必须分别加在两个羰基的氧上。可见,选择性近乎专一的催化剂制备以及反应工艺的研究一直是这个重要反应研究的关键核心,获得唯一的加氢产物是实现过氧化氢高效制备追求的最大目标。